
Molaridad de un Líquido
En un laboratorio, las cosas son diferentes, en Química la mayoría de los cálculos usan unidades de masa y muy pocos en volumen, por esta razón, cuando se nos presentan estos problemas a veces no se sabe que hacer, la solución esta detrás de la densidad.
Recordemos que la densidad es una relación que existen entre la masa de un compuesto o solución y su volumen, de esta manera será posible calcular la masa para realizar los cálculos necesarios de la molaridad. La densidad de nuestra sustancia podremos encontrarla en la ficha técnica o en el envase, recordar eso. Veamos un ejercicio.
Ejercicio resuelto.
Se usa 85 ml de HCl para preparar 500 ml de una solución, Calcula la Molaridad si la densidad del HCl es de 1.49 g/ml.
Datos
Soluto = 85 ml
Volumen = 500 ml = 0.5 L
Densidad = 1.49 g/ml
Fórmulas
Masa = Densidad x Volumen
n = Masa / MM
M = n / V
Solución
Calculamos la masa del HCl usando su densidad
Masa = Densidad x Volumen
Masa = (1.49 g/ml)(85 ml)
Masa = 126.65 g
Calculamos la Masa Molecular del HCl
H: 1 g/mol
Cl: 35.45 g/ mol
---------------------
MM = 36.45 g/mol
Calculamos los moles
n = Masa / MM
n = (126.65 g) / 36.45 g/mol
n = 3.4746 mol
Calculamos la Molaridad
M = n/V
M = (3.4746 mol) / (0.5 L)
M = 6.94 mol/L
Aunque una solución al Aprox. 7 M no se ocupa generalmente, el procedimiento para hacer los cálculos están plasmados aquí.
Otra forma de calcularlo
Incluso podemos incorporar la densidad y los número de moles dentro de la ecuación de la molaridad para que éste sea un calculo directo;
M = ((Densidad x Volumen HCl) / (MM)) / (Volumen Sol. (L))
Densidad = 1.49 g/mol
Volumen HCl = 85 ml
MM del HCl = 36.45 g/mol
Volumen Sol (L) = 0.5 L
Desventaja: Si no sabes usar paréntesis, fallarás
Veamos cómo quedaría la ecuación
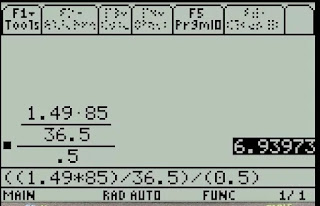 |
| Nótese cómo existen dos divisiones, una sobre otra, el uso de paréntesis debe ser la correcta |



No hay comentarios.
SI DESEAS AYUDA Y HACES UN COMENTARIO ANONIMO, DEJANOS UN DATO PARA PODER CONTACTARTE Y PODER APOYARTE