
HI + H2SO4 → H2S + I2 + H2O
3 - H - 4
1 - I - 2
1 - S - 1
4 - O - 1
NO está balanceada

|
|
Cada valencia en un compuesto debe sumar cero, ¿Quieres saber más?, mira
el enlace de abajo |
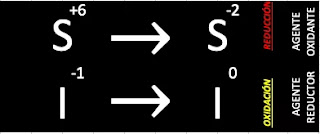
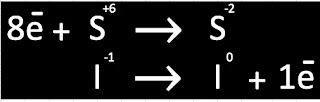
*¿No sabes cómo se coloca cada número de oxidación?Paso 3. Identificar y separa los elementos que se reducen y se oxidan respectivamente, colocar cuantos electrones de diferencia hay entre cada uno de ellos.
▷ IDENTIFICAR ✅ EL NÚMERO DE OXIDACIÓN EN UN COMPUESTO TRUCO ❤️
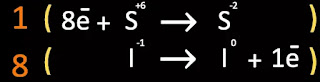
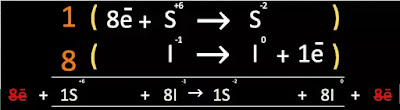
Paso 6. Semireacción. Multiplique los coeficientes por toda la reacción
parcial
8HI + 1H2SO4 → 1H2S + 8I2 + H2O
10 - H - 4
8 - I - 2
1 - S - 1
4 - O - 1
NO está balanceada
8HI + 1H2SO4 → 1H2S + 4I2 + H2O
10 - H - 4
8 - I - 8
1 - S - 1
4 - O - 1
NO está balanceada
Ajustamos el Hidrógeno ajustando en la molécula de agua, colocando un 4
8HI + 1H2SO4 → 1H2S + 4I2 + 4H2O
10 - H - 10
8 - I - 8
1 - S - 1
4 - O - 4
Balanceada
Como ves, no hizo falta ajustar al oxígeno.



No hay comentarios.
SI DESEAS AYUDA Y HACES UN COMENTARIO ANONIMO, DEJANOS UN DATO PARA PODER CONTACTARTE Y PODER APOYARTE