
Balance por el Método REDOX reacción de descomposición
Antes de comenzar el procedimiento de balanceo redox para la reacción HNO3
= NO + H2O + O2, es crucial identificar las especies oxidantes y reductoras,
asignar los números de oxidación y dividir la reacción en semirreacciones.
Al enfrentarte a obstáculos, es común lidiar con la complejidad de ajustar
el balance de oxígeno e hidrógeno, así como garantizar la igualdad en la
cantidad de electrones transferidos. Es fundamental seguir una secuencia
lógica, ajustar las cargas mediante la adición de electrones y equilibrar
cuidadosamente cada especie química. Mantén la atención en la conservación
de la masa y carga a lo largo del proceso para superar desafíos y alcanzar
una ecuación redox balanceada de manera precisa.
Video Tutorial
Reacción química
HNO3 → NO + H2O + O2
Paso 1. Colocar el número de oxidación a cada elemento
Como se menciona en el video, iniciar colocando un -2 como número de
oxidación al oxígeno resulta ser mas rápido, para este ejemplo el oxígeno
molecular maneja número de oxidación 0 por estar solo como compuesto
Paso 2. Identificar qué elemento tiene una variación en su número de oxidación.
Al mismo tiempo hacemos un balance de esta mini reacción, ajustando el Oxígeno
Paso 3. Identificar quien se oxida y quien se reduce, así también como el agente reductor y el agente oxidante.
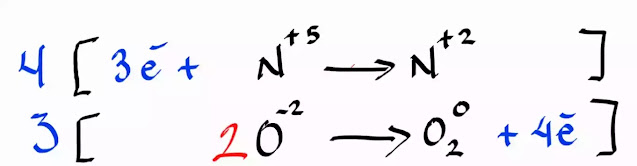
Paso 4. Realizar el balance de electrones
Ahora el balance de electrones. si tienes dudas de cómo hacer el balance
de electrones te recomiendo veas esto primero;
En 2O-2→O2, el oxígeno (O) se reduce, ganando electrones. Aquí, se colocan 4 electrones en el lado de los productos para igualar la variación en la carga.
Paso 5. Cruzar los coeficientes
Paso 6. Multiplicar los coeficientes y obtener la semi reacción
Paso 7. Sustituir los coeficientes en la reacción química original
Por orden general para el compuesto del reactivo usaremos el coeficiente
del Nitrógeno, colocamos los coeficientes, y ajustamos la reacción química
si es necesario
4HNO3 → 4NO + H2O + 3O2
4 - N - 4
4 - H - 2
12 - O - 11
NO BALANCEADA
Ahora colocamos un 2 a la molécula del agua para balancear la
reacción
4HNO3 → 4NO + 2H2O + 3O2
4 - N - 4
4 - H - 4
12 - O - 12
BALANCEADA




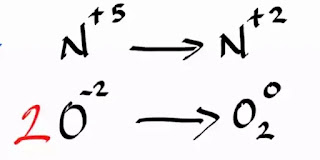



No hay comentarios.
SI DESEAS AYUDA Y HACES UN COMENTARIO ANONIMO, DEJANOS UN DATO PARA PODER CONTACTARTE Y PODER APOYARTE