
Produce muchas moles de agua (14)
Balancear por el método REDOX suele ser complicado si no entiendes algunos
conceptos importantes; principalmente al hacer el balance de electrones, es
por ello que te dejaré un enlace para que comprendas ese tema.
Video tutorial
Reacción química a balancear
NH3 + H2SO4 → S + HNO3 +
H2O
Estado de oxidación
Colocamos el número de oxidación a cada elemento, hasta que la suma sea
cero
¿Quieres aprender a colocar números de oxidación?
Qué elemento cambió su estado de oxidación
Observemos cada elemento, atentamente en el número de oxidación y
separemos aquellos dos que sufrieron un cambio.
Quién se oxida y quien se reduce
Recuerda identificar el que se reduce primero, pues la propia
palabra da un significado y fácil de entender
- El N se oxida, pues su valencia aumenta de -3 a +5
- El S se reduce , pues su valencia disminuye de +6 a 0
Agente reductor y agente oxidante
El agente reductor es el que se oxida (Nitrógeno)
El agente oxidante es el que se reduce (Azufre)
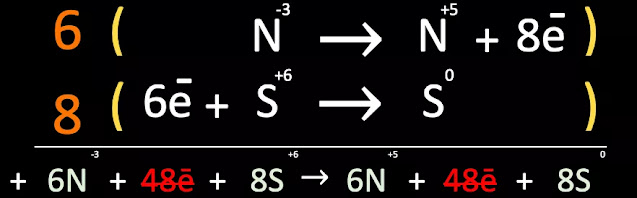
Balance de electrones
Como hacer la semireacción
Tomamos los coeficientes del balance de electrones (el 6 y el 8) y los
cambiamos de fila;
Ahora multiplicamos cada coeficiente por su respectiva fila, respetando los reactivos y productos de la reacción química;
Balance parcial
Colocamos cada coeficiente en el orden que la semireacción no ha dado y
comprobamos si la reacción química está balanceada;
6NH3 + 8H2SO4 → 8S + 6HNO3 + H2O
6 - N - 6
34 - H - 8
8 - S - 8
32 - O - 19
NO BALANCEADA
La reacción no quedo balanceada, tendremos que hacer el ajuste
pertinente. Los elementos no balanceados es el H, O, de estos dos
daremos prioridad al H, y despues al O.
Ajustamos a la molécula de agua colocando un 14, pues 14 x 2 = 28, y 28
+ 6 de H que tiene el ácido nítrico suman 34. El oxigeno su ajusta en
automático.
6NH3 + 8H2SO4 → 8S + 6HNO3 + 14H2O
6 - N - 6
34 - H - 34
8 - S - 8
32 - O - 32
BALANCEADA







No hay comentarios.
SI DESEAS AYUDA Y HACES UN COMENTARIO ANONIMO, DEJANOS UN DATO PARA PODER CONTACTARTE Y PODER APOYARTE